Cho 22,2g (canxi clorua) CaCl2 pứ với 200ml dd Na2SO4 dư(1,55g/ml) tính nồng độ phần trăm( c%) của dd muối thu được.

Những câu hỏi liên quan
cho 43,5gam MnO2 tác dụng hết với 250gam dd HCl thu được khí A. dẫn khí A qua 400ml dd NaOH 5M thu được dd B
a) tính nồng độ mol các muối trong dd B
b) Tính C% của dd HCl ban đầu (dùng dư 10% so với phản ứng)
MnO2+4HCl->MnCl2+H2O+Cl2
0,5---------2------0,5--------0,5---0,5
Cl2+2NaOH->NaClO+NaCl+H2O
0,5-----1--------0,5----------0,5------0,5
n MnO2 =\(\dfrac{43.5}{87}\)=0,5 mol
n NaOH=5.0,4=2 mol
=>NaOH dư :0,1 mol
=>CM NaCl= CM NaClO =\(\dfrac{1}{0,4}\)=2,5M
=>CM NaOH dư =1\(\dfrac{1}{0,4}\)=2,5M
b)
C%HCl =\(\dfrac{2.36,5}{250}100\)=29,2%
dùng dư 10%
=>C%HCl=29,2+10=39,2%
Đúng 0
Bình luận (2)
Hỗn hợp X gồm KOH,NaOH,Mg(OH)2 trong đó số mol của KOH=số mol của NaOH . Hòa tan X bằng dd H2SO4 9,8% thu được dd Y chỉ chứa muối sunfat trung hòa trong đó nồng độ% của Na2SO4 là 2,646%. Tính nồng độ mol % các muối còn lại trong dd Y
44. Nhúng một thanh kẽm sạch khối lượng 10 gam vào 250ml dd AgNO3 0,3M (D=1,13gam/ml) đến khi lượng muối bạc phản ứng hết
a/ Lấy thanh kẽm ra rửa nhẹ,làm khô cân nặng được bao nhiêu gam
b/ Tính nồng độ phần trăm dd muối thu được sau phản ứng.
a)
$n_{AgNO_3} = 0,3.0,25 = 0,075(mol)$
$Zn + 2AgNO_3 \to Zn(NO_3)_2 + 2Ag$
Theo PTHH :
$n_{Zn\ pư} = \dfrac{1}{2}n_{AgNO_3} = 0,0375(mol)$
$n_{Ag} = n_{AgNO_3} = 0,075(mol)$
Sau pư : $m_{thanh\ kẽm} = 10 - 0,0375.65 + 0,075.108 = 18,6625(gam)$
b)
Sau pư : $m_{dd} = 0,0375.65 + 250.1,13 - 0,075.108 = 276,8375(gam)$
$n_{Zn(NO_3)_2} = n_{Zn\ pư} = 0,0375(mol)$
$C\%_{Zn(NO_3)_2} = \dfrac{0,0375.189}{276,8375}.100\% = 2,56\%$
Đúng 3
Bình luận (0)
cho 5.4 gam Nhôm tác dụng vừa đủ với 200gam dung dịch HCl
a) tính thể tích khí H2 sinh ra (đktc)
b) Tính nồng độ phần trăm của dung dịch HCl đã dùng
c) tính nồng độ phần trăm của dung dịch thu được sau phản ứng
Theo gt ta có: $n_{Al}=0,2(mol)$
$2Al+6HCl\rightarrow 2AlCl_3+3H_2$
a, Ta có: $n_{H_2}=0,3(mol)\Rightarrow V_{H_2}=6,72(l)$
b, Ta có: $n_{HCl}=0,6(mol)\Rightarrow \%C_{HCl}=10,95\%$
c, Sau phản ứng dung dịch chứa 0,2 mol AlCl3
Suy ra $\%C_{AlCl_3}=13,03\%$
Đúng 1
Bình luận (0)
Cho 18.5 gam hỗn hợp X gồm Fe, Zn, Cu vào dung dịch H2SO4 loãng dư thu được 4,48 lit khí (dktc). Nếu cũng cho lượng hỗn hợp X trên vào H2SO4 đặc nóng, eư thì thu được 7,84 lit khí SO2 (dktc)a) Tính thành phần trăm theo khối lượng của các kim loại trong hỗn hợp đầub) Dẫn lượng khí So2 thu được đi qua 200ml dd KOH 1M. Tính khối lượng và nồng độ mol các chất trong dd sau phản ứng
Đọc tiếp
Cho 18.5 gam hỗn hợp X gồm Fe, Zn, Cu vào dung dịch H2SO4 loãng dư thu được 4,48 lit khí (dktc). Nếu cũng cho lượng hỗn hợp X trên vào H2SO4 đặc nóng, eư thì thu được 7,84 lit khí SO2 (dktc)
a) Tính thành phần trăm theo khối lượng của các kim loại trong hỗn hợp đầu
b) Dẫn lượng khí So2 thu được đi qua 200ml dd KOH 1M. Tính khối lượng và nồng độ mol các chất trong dd sau phản ứng
Câu 1: cho 1,68g (canxi ôxit) CaO hòa tan hoàn trong 300g H2O. tính nồng độ phần trăm (C%) của dd thu được.Câu 2: Cho 12 gam đồng ôxit (CuO) tác dụng hết với 200ml dd H2SO4, khối lượng riêng 1,98g/ml. tính nồng độ C% của dd thu được.Câu 3: Cho 22,2 g (canxi clorua) CaCl2 pứ với 200ml dd Na2SO4 dư (d1,55g/ml) tính nồng độ phần trăm (c%) của dd muối thu được.Câu 4: Cho 200g dd H2SO4, 14,% tác dụng với Al dư. Tính khối lượng muối Al2(SO4)3thu được?Câu 5: Cho 300 ml dd H2SO4 0,1M tác dụng hết vớ...
Đọc tiếp
Câu 1: cho 1,68g (canxi ôxit) CaO hòa tan hoàn trong 300g H2O. tính nồng độ phần trăm (C%) của dd thu được.
Câu 2: Cho 12 gam đồng ôxit (CuO) tác dụng hết với 200ml dd H2SO4, khối lượng riêng 1,98g/ml. tính nồng độ C% của dd thu được.
Câu 3: Cho 22,2 g (canxi clorua) CaCl2 pứ với 200ml dd Na2SO4 dư (d=1,55g/ml) tính nồng độ phần trăm (c%) của dd muối thu được.
Câu 4: Cho 200g dd H2SO4, 14,% tác dụng với Al dư. Tính khối lượng muối Al2(SO4)3thu được?
Câu 5: Cho 300 ml dd H2SO4 0,1M tác dụng hết với Al tạo thành (muối nhôm sunfat) Al2(SO4)3. tính nồng độ của dd Al2(SO4)3 trên?
Câu 1:
Khối lượng CaO: 
Số mol CaO:
Pt:
 số mol Ca (OH)2
số mol Ca (OH)2
Vậy khối lượng Ca(OH)2tạo thành: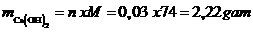
Vậy mct = 2,22 gam
 Mà
Mà 
Vậy nồng độ phần trăm Ca(OH)2: 
Đúng 0
Bình luận (0)
Câu 2:
+ Khối lượng riêng  khối lượng dd H2SO4 là
khối lượng dd H2SO4 là 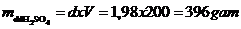
+ 
Số mol CuO: 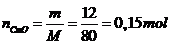
 Pt:
Pt: 

 Khối lượng
Khối lượng 
Vậy khối lượng chất tan: mct = 24 gam
Mà 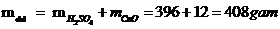
Vậy nồng độ phần trăm: 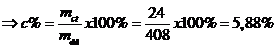
Đúng 0
Bình luận (0)
Câu 3:
+Khối lượng riêng 
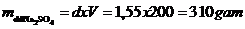 (1)
(1)

số mol
Pt:

số mol nước muối NaCl tạo thành:
Khối lượng NaCl:  (2)
(2)

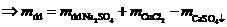 (*) (vì
(*) (vì kết tủa và bị vớt ra làm khối lượng dd giảm)
kết tủa và bị vớt ra làm khối lượng dd giảm)

 (3)
(3)
Từ 1,2,3 thay vào * ta có: 
Vậy nồng độ phần trăm dd muối NaCl : 
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
hòa tan hoàn toàn 9,6 gam hỗn hợp mgco3 cần 100 gam dd hcl 14,6%
a) tính thể tích mỗi khi thu được
b) tính nồng độ phần trăm của dd sau phản ứng
Ta có ptpu
MgCO3+ 2HCl ----> MgCl2 + H2O+ CO2
\(n_{MgCO3}\)= \(\frac{9,6}{84}\)= \(\frac{0,8}{7}\) ( mol)
\(m_{HCl}\)= \(\frac{14,6}{100}.100\)= 14,6(g)
=> \(n_{HCl}\)= \(\frac{14,6}{36,5}=0,4\left(mol\right)\)
Theopt ta thấy sau phản ứng HCl dư và dư \(\frac{1,2}{7}\) mol==> m dư= 6,26 (g)
=> \(n_{CO2}\)= \(n_{MgCO3}\)= \(\frac{0,8}{7}\) mol
=> \(V_{CO2}\)= \(\frac{0,8}{7}.22,4=2,56\left(l\right)\)
b)
Ta có \(m_{CO2}\)= \(\frac{0,8}{7}.44=\frac{35,2}{7}\left(g\right)\)
\(m_{H2O}\)= \(\frac{0,8}{7}.18=\frac{14,4}{7}\)( g)
\(m_{MgCl2}\)= \(\frac{0,8}{7}.95=\frac{76}{7}\)(g)
=> \(m_{dd_{MgCl2}}\)= (9,6+100)-( \(\frac{49,6}{7}\))= 102,5(g)
=> \(C\%_{MgCl2}\)= \(\frac{\frac{76}{7}}{102,5}\). 100%= 10,6 ( %)
\(C\%_{HCl_{dư}}\)= \(\frac{6,26}{102,5}.100\)=6,107 ( %)
Đúng 0
Bình luận (0)
đề có hơi vô lý một tý nha: hỗn hợp thì phải 2 chất trở lên, nhưng trong đề chỉ có mỗi MgCO3....Đề ghi vậy thì anh làm theo đề nha
mHCl=(14.6*100)/100=14.6g=>nHCl=0.4 mol
nMgCO3=9.6/84=4/35\(\approx\) 0.114mol
theo pthh,HCl dư 2/7 mol=>mHCl dư=73/7g
MgCO3+2HCl --> MgCl2 + CO2+H2O
4/35 0.4 4/35 4/35
a)Vco2=(4/35)*22.4=2.56l
b)C%HCl dư=(73/7)/100*100=76/7\(\approx\) 10.42%
mMgCl2=4/35*95=76.7g
C%MgCl2=(76.7)/100*100=76/7\(\approx\) 10.85%
Chúc em học tốt!!1
Đúng 0
Bình luận (0)
cho 100g dd HCl 50% vào 200g dd HCl 50%. Tính nồng độ phần trăm của dd HCl sau khi pha.
mHCl = 100 . 50% + 200 . 50% = 150 (g)
mddHCl = 100 + 200 = 300 (g)
C%ddHCl = 150/300 = 50%
Đúng 2
Bình luận (0)
Cho Al tác dụng với 200ml dung dịch axit clohiddric 1M (Ddung dịch HCL= 1,8g/ml)
A) tính thể tích khí thoát ra ở ĐKTC
B) tính Khối lượng nhôm tham gia phản ứng
C) tính nồng độ% của dung dịch muối thu được( thể tích dung dịch không thay đổi)
a.Ta có: nHCl=1.\(\frac{200}{1000}\)=0,2(mol)
Ta có phương trình 2Al + 6HCl -----> 2AlCl3 + 3H2 (1)
Theo phương trình: 2 mol 6 mol 3 mol
Theo đề: x mol 0,2 mol 0,1 mol
=> V\(H_2\)=0,1.22,4=2,24(l)
b. Từ pt (1), ta có:
mAl=x.27=\(\frac{0,2.2}{6}\).27=1,8(g)
c.Từ pt (1), ta có: mHCl=0,2. (1+35,5)=7,3(g)
mdd=\(\frac{200}{1000}.22,4.18=80,64\left(g\right)\)
=>C%=\(\frac{7,3}{80,64}.100\%=9,1\%\)
Ungr hộ nha!
Đúng 0
Bình luận (0)



















